La inercia terapéutica en el tratamiento del colesterol dificulta el control en pacientes de alto y muy alto riesgo, debido a la subestimación de riesgos y estrategias conservadoras. Romper esta inercia permite reducir el c-LDL y prevenir eventos cardiovasculares a largo plazo, según estudios recientes.
Romper Inercias
- La inercia en el tratamiento del colesterol se ha relacionado con una falta de control en los pacientes de alto y muy alto riesgo.
- La resistencia al cambio en la estrategia clínica puede derivarse de la subestimación de los riesgos o del sobreúso de estrategias de “espera y ver” en lugar de avanzar a combinaciones terapéuticas o intensificaciones.
- Romper esta inercia puede ayudar a reducir el LDL y disminuir los eventos cardiovasculares a largo plazo, tal como se ha mostrado en los estudios.
Factores responsables de la inercia1

1. Causas relacionadas con el medicamento (24,6%)
– Se ha llegado a dosis máxima tolerada (posible) (10,3%)
– No se modifica el tratamiento por aparición de efectos adversos (10,9%)
– Mialgia sin elevación de CK (5,7%)
– Elevación de CK (2,9 %)
– Elevación transaminasas (3 veces límite superior de la normalidad) (1,1%)
– Intolerancia a fármacos (5,7%)

2. Causas relacionadas con el médico (43,4%)
– Dificultad de prescripción de ciertos fármacos (1,1%)
– Inercia terapéutica 34 (19,4%)
– No seguimiento de las Guías (5,1%)
– Desprescripción por parte del médico de familia (6,9%)
– Desprescripción por parte de otro especialista (0,6%)
– Médico considera que se ha alcanzado el objetivo terapéutico (13,7%)

3. Causas relacionadas con el paciente (46,9%)
– Comorbilidad (5,7%)
– Polifarmacia (2,9%)
– Incumplimiento terapéutico (31,4%)
– Incumplimiento en el seguimiento (11,4%)
– No lo puede financiar (2,9%)
Medidas para disminuir la inercia terapéutica2
1. Promover la formación continuada.
2. Marcar claramente los objetivos terapéuticos.
3. Establecer auditorias.
4. Implantar la historia clínica informatizada con alertas.
5. Favorecer o incentivar la investigación en este campo.
6. Divulgar las guías de práctica clínica mediante algoritmos y esquemas.
7. Crear incentivos motivadores.
8. Organizar la asistencia.
9. Mejorar la relación médico-paciente.
10. Implicar a otros agentes sanitarios en el problema.
Tratamiento orientado a objetivos. Dónde queremos llegar.
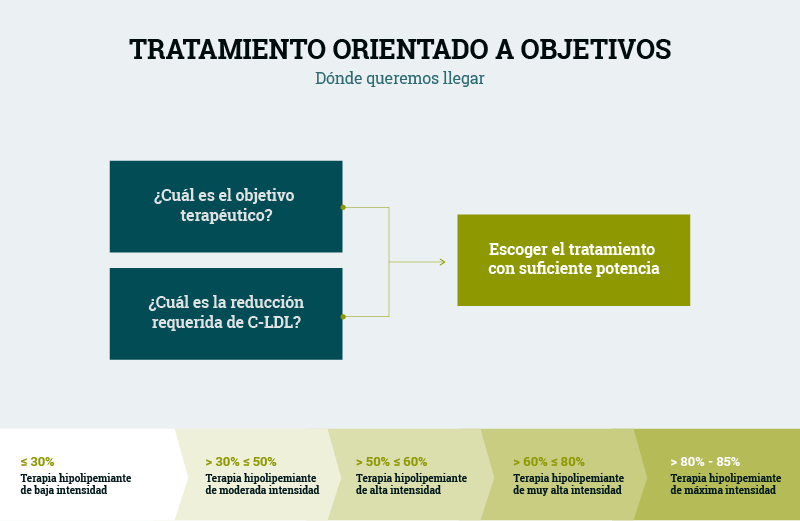
✔️ Para la prescripción de una terapia farmacológica3, se recomienda seguir una estrategia de planificación terapéutica orientada a un objetivo de c-LDL desde el primer momento.
✔️ Se debe tener en cuenta el c-LDL basal y el objetivo de c-LDL según el riesgo vascular del paciente para calcular la reducción porcentual requerida.
✔️ La eficacia terapéutica del tratamiento hipolipemiante nos llevará a la consecución de los objetivos marcados. Para ello, se pueden utilizar tablas (Tabla 1) o programas informatizados que nos calculan los fármacos y las dosis necesarias para alcanzar el objetivo.
Tabla 1
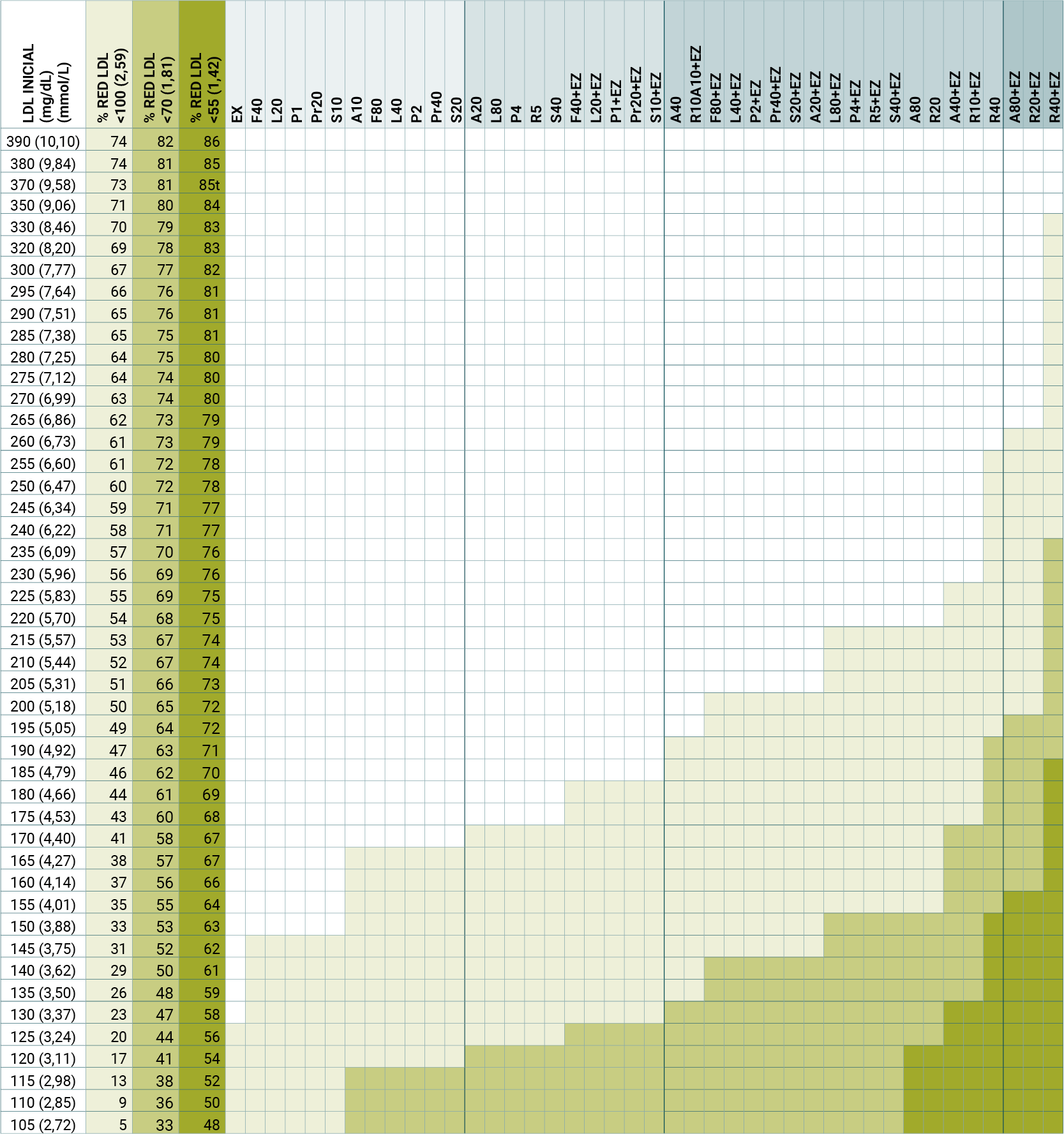
Tabla extraída de Masana L, Plana N. Update of therapeutic planning tables oriented towards obtaining therapeutic objectives. Clin Investig Arterioscler. 2019;31:271–7.
Objetivos3,4
Según el riesgo cardiovascular:
- Personas aparentemente sanas (sin ECV, DM, ERC ni HF) con riesgo bajo-moderado: objetivo c-LDL < 115 mg/dl
Riesgo bajo-moderado según SCORE2-(OP) (tabla 2)
≥ 2,5% - < 7,5% (si < 50 años),
≥ 5% - <10% (si 50-69 años)
≥ 7,5% - <15% (si 70 o más años)
- Personas aparentemente sanas (sin ECV, DM, ERC ni HF) con riesgo alto: c-LDL < 70 mg/dl + reducción del 50% del valor basal
Riesgo alto según SCORE2-(OP)
≥ 2,5% - < 7,5% (si < 50 años),
≥ 5% - <10% (si 50-69 años)
≥ 7,5% - <15% (si 70 o más años)
- Personas aparentemente sanas con muy alto riesgo o enfermedad cardiovascular ateromatosa (prevención secundaria): c-LDL < 55 mg/dl + reducción del 50% del valor basal
Riesgo alto según SCORE2-(OP)
≥ 7,5% (si < 50 años),
≥ 10% (si 50-69 años)
≥ 15% (si 70 o más años)
Tabla 2

Tabla extraída de SCORE2 working group and ESC Cardiovascular risk collaboration. SCORE2 risk prediction algorithms: new models to estimate 10-year risk of cardiovascular disease in Europe. Eur Heart J. 2021 Jul 1;42:2439-2454. doi: 10.1093/eurheartj/ehab309.
Eficacia del tratamiento hipolipemiante (tabla 3):
Baja intensidad: reducción de c-LDL < 30%
Moderada intensidad: reducción de c-LDL > 30 y < 50%
Alta intensidad: reducción de c-LDL >50 y < 60%
Muy alta intensidad: reducción de c-LDL >60 y < 80%
Máxima intensidad: reducción de c-LDL > 80%
Tabla 3
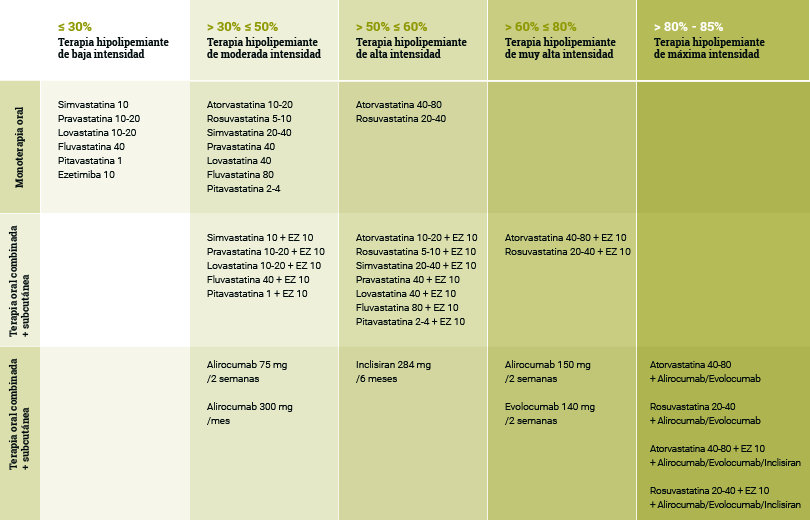
"*Tabla creada por la Dra. Cristina Soler a partir de datos publicados"
Tratamiento combinado de entrada
- El uso de combinaciones de inicio5, como estatinas con ezetimiba, ácido bempedoico o inhibidores de PCSK9, ayuda a lograr reducciones rápidas y sostenidas de c-LDL, minimizando el riesgo de eventos cardiovasculares tempranos.
- La evidencia sugiere que estas combinaciones son especialmente efectivas en pacientes de muy alto riesgo y pueden prevenir la progresión de la aterosclerosis al atacar múltiples mecanismos de formación de placas desde etapas iniciales.
- Especialmente en pacientes con cifras muy elevadas de c-LDL (por ejemplo, en HF) o objetivos de reducción muy bajos (ECV establecida) el tratamiento con estatinas en monoterapia no tendrá eficacia suficiente (Tabla 1) y deberemos empezar directamente con tratamiento combinado.
- El uso de combinaciones aumenta además la adherencia al tratamiento.
Tiempo de control. Ni precipitarse ni relajarse.
Controlar el tiempo en la evaluación del tratamiento es crucial.
La investigación sugiere que un seguimiento de cada 3 a 6 meses tras la intensificación permite ajustar y optimizar la terapia sin precipitar cambios innecesarios.
Sin embargo, retrasar la intervención también puede resultar en progresión de la enfermedad, por lo que debe existir un balance entre un control adecuado sin prolongar el tiempo entre evaluaciones, sobre todo en pacientes de alto y muy alto riesgo.
Autora:

Dra. Cristina Soler Ferrer
Médico especialista en Medicina Interna, Hospital de Santa Caterina, Girona.
PCSK9: proproteína Convertasa Subtilisina/Kexina tipo 9
c-LDL: colesterol LDL
ECV: enfermedad cardiovascular
DM: diabetes mellitus
ERC: enfermedad renal crónica
HF: hipercolesterolemia familiar hereditaria
CK: creatina quinasa
- Morales C, Soler C, grupo de Investigadores EROMOT-XULA. Causes of failure to achieve the low density lipoprotein cholesterol therapeutic target in patients with high and very high vascular risk controlled in Lipid and Vascular Risk Units. EROMOT study. Clin Investig Arterioscler. 2018 Jan-Feb;30(1):1-9.
- Blasco M, Pérez-Martínez P, Lahoz C. of the Spanish Society of Arteriosclerosis to reduce therapeutic inertia. Clin Investig ArteriDecalogueoscler. 2017 Sep-Oct;29(5):218-223
- “Guia clínica sobre el maneig de les dislipèmies per la prevenció cardiovascular de la XULA.” Lluís Masana, Cristina Soler, XULA [Editors científics]. Girona: Xarxa d’Unitats de Lípids de Catalunya, 2022. ISBN 978-84-09-43261-5
- Mach F, Baigent C, Catapano AL et al. ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the manage- ment of dyslipidaemias: lipid modification to reduce cardio- vascular risk. Eur Heart J. 2020;41:111-188
- Ray KK, Reeskamp LF, Laufs U, Banach M, Mach F, Tokgözoğlu LS, Connolly DL, Gerrits AJ, Stroes ESG, Masana L, Kastelein JJP. Combination lipid-lowering therapy as first-line strategy in very high-risk patients. Eur Heart J. 2022 Feb 22;43(8):830-833. doi: 10.1093/eurheartj/ehab718. PMID: 34636884
Contenido recomendado
MAT-ES-2500864 v1 Mayo 2025








-sea.png/jcr:content/consenso-lp(a)-sea.png 767w, /.imaging/webp/sanofi-platform/imgAutox300/dam/ak9demia-es/actualidad/consenso-lpa-sociedad-espanola-arteriosclerosis/consenso-lp(a)-sea.png/jcr:content/consenso-lp(a)-sea.png 1200w)





